|
������Ӧ��Ƥ�ף�atopic dermatitis��AD����һ��������֢�Լ�����ͨ����Ƥ�����ʽ���֡�����WHO���ݣ�ȫ��Ŀǰ������2.5�����ܵ�AD�����š�AD�����Ϊ����7�������������������ʿ�����25%����Ŀǰ�����о�֤��AD�ڳ��˵ķ�����Ҳ���Դ�10%��Ŀǰȫ��AD�����г��ռ��Ѵ������Ԫ����ΪIL-4Rα��������·����DZ�ڵ�Best-in-Class�����˵µ�CBP-201������δ�����к�Ϊ����AD�����г����ذ���Ʒ��
��������CBP-201��CBP-307ͬ��Ҳ�ǿ��˵����еĺ��ĺ�ѡ��Ʒ֮һ��
������ͨ�ƾ��˽��CBP-307���ʰ���-1-��������1��S1P1�������͵ڶ���������������һ���ڵ���Tϸ���˶�����������õ�G����ż�����壨GPCR����
����ֵ��һ����ǣ�CBP-307��ʹ�ÿ��˵�ר��Tϸ��ɸѡƽ̨���ֵģ������������ٴ��ϻ�����ǿ��S1P1������������������������ʡ�����������ɵ�I�������˫ä����ο�������о��У�CBP-307���ֳ���Ч��Tϸ�����ڻ��ԺͰ�ȫ�ԡ�
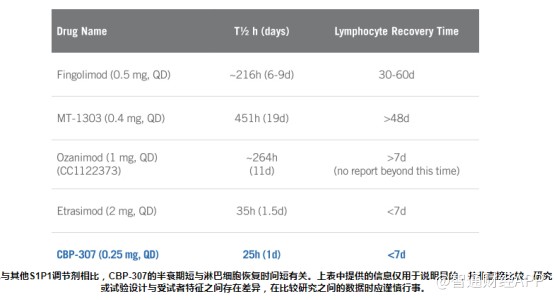
�����й�����ʾ��CBP-307Ŀǰ���ڽ�������II���о���������������ض������Խ᳦�����ضȿ��������ߵ���Ч�Ͱ�ȫ�ԡ�
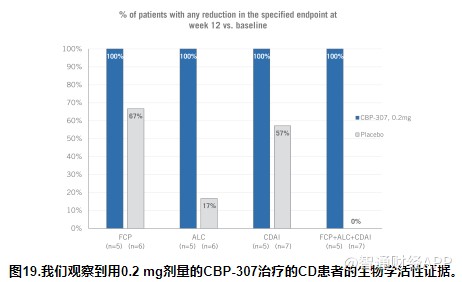
�������⣬���˵»���ͬ���ƽ�CBP-174С���Ӻ�ѡҩ�CBP-233����IL-33�Ŀ�����ٴ�ǰ��Ŀ���������ƶ������ص���֢�Լ�����Ŀǰ�������о��д����ٴ�ǰ�Ρ�
�����ڲ����棬������ڶഴ��ҩ�з���˾���ƣ����˵�Ŀǰ����������Դ�����з�����������2019���2020�꣬�ù�˾�з����÷ֱ�Ϊ1.06��Ԫ������ң���λ��ͬ����1.51��Ԫ���з����õ������빫˾�ٴ�������Ȼ�������һ�¡�
�������ң�����ȥ����ĩ�����˵³��е��ֽ��ֽ�ȼ��P����Ͷ���ܼ�Լ10.23��Ԫ����˵����˾Ŀǰ�г�����ֽ��Թ������Ĺ�˾��Ӫ���з�Ͷ�롣
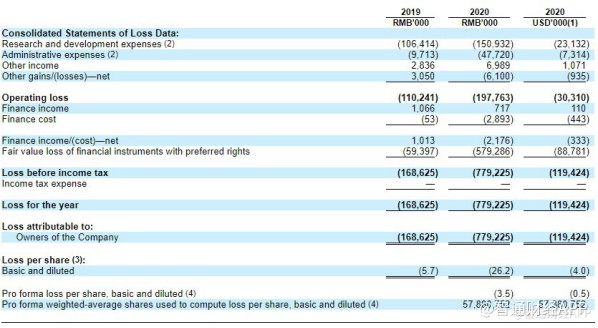
������Ŀǰ�Ľڵ�������Ͷ���߹�ע���˵µ�����Ӧ��Ҫ����������з��Ľ��ȼ���Ʒ�������档
������Ŀǰ�з���������CBP-201Ϊ�������Ӧ��Ӧ֢��ҪΪ��Ӧ��Ƥ�ס��ڹ����г���AD���߷�����ԼΪ10%��Ԥ�������ڵĻ�����Ⱥ��
�������г����������������������AD������ҩ��ŵ��/����Ԫ��AD�Ʒ�Dupilumab��Dupixent����������Eucrisa��ȥ������ڹ��ڻ������С����ڹ��ڣ�Ŀǰ�����ٴ��ε�AD��ҩ��Ҫ������Z��ҩ����ܿ����ᣨJAK���Ƽ���������SHR0302��JAK���Ƽ���������Eucrisa��PDE4���Ƽ�����������Heymay808������������ɶ���ŵ�ǵȶ����ҵ���뿵�˵�CBP-201һ��������IL-4Rα���塣
�����ɼ������˵����з������ϲ����������ƣ���������δ���г�������Χ������£���ʵ�ƽ����IJ�Ʒ����ҵ�������Ǿ�����˾��ֵ����Ĺؼ��㡣
������Դ����ͨ�ƾ��� ��2ҳ ��һҳ [1] [2] ��������: ���˵� |